Dengan menggunakan teori VSEPR maka kita dapat meramalkan bentuk geometri suatu molekul. Dalam artikel ini maka akan di contohkan menentukan bentuk geometri molekul XeF2, XeF4, dan XeF6. Diantara molekul-molekul tersebut ada yang memiliki pasangan elektron bebas dan ada yang tidak, jadi molekul-molekul tersebut adalah contoh yang bagus untuk lebih memahami teori VSEPR.
Pertama kita harus mementukan struktur lewis masing-masing molekul. Xe memiliki jumlah elektron valensi 8 sedangkan F elektron valensinya adalah 7.(lihat gambar dibawah)

Struktur Lewis XeF2 seperti gambar sebelah kiri, dua elektron Xe masing-masing diapakai untuk berikatan secara kovalen dengan 2 atom F sehingga meninggalkan 3 pasangan elektron bebas pada atom pusat Xe. Hal yang sama terjadi pada molekul XeF4 dimana 4 elektron Xe dipakai untuk berikatan dengan 4 elektron dari 4 atom F, sehingga meninggalkan 2 pasangan elektron bebas pada atom pusat Xe.


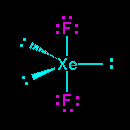
Lihat gambar diatas XeF2 memiliki 2 pasangan elekktron terikat (PET) dan 3 pasangan elektron bebas (PEB) jadi total ada 5 pasangan elektron yang terdapat pada XeF2, hal ini menandakan bahwa geometri molekul atau kerangka dasar molekul XeF2 adalah trigonal bipiramid. Karena terdapat 3 PEB maka PEB ini masing masing akan menempati posisi ekuatorial pada kerangka trigonal bipiramid, sedangkan PET akan menempati posisi aksial yaitu pada bagian atas dan bawah. Posisi inilah posisi yang stabil apabila terdapat atom dengan 2 PET dan 3 PEB sehingga menghasilkan bentuk molekul linear. Jadi bentul molekul XeF2 adalah linier.(lihat gambar dibawah).

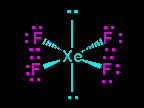
Lihat gambar strutur lewis XeF4 memiliki 4 pasangan elekktron terikat (PET) dan 2 pasangan elektron bebas (PEB) jadi total ada 6 pasangan elektron yang terdapat pada XeF4, hal ini menandakan bahwa geometri molekul atau kerangka dasar molekul XeF4 adalah oktahedral. Karena terdapat 2 PEB maka PEB ini masing masing akan menempati posisi aksial pada kerangka oktahedral, sedangkan PET akan menempati posisi ekuatorial. Posisi inilah posisi yang stabil apabila terdapat atom dengan 4 PET dan 2 PEB sehingga menghasilkan bentuk molekul yang disebut segiempat planar. Jadi bentul molekul XeF2 adalah segiempat planar.(lihat gambar dibawah).

Tidak ada komentar:
Posting Komentar